Aujourd’hui on va faire un petit billet d’actualité sur le coronavirus, et surtout sur l’armada de protéines qui lui ont permis de conquérir le monde en quelques mois.
Les coronavirus sont une famille de virus qui doit son nom à la couronne de protéines qui entoure la membrane de ceux-ci lorsqu’on les observe au microscope électronique. Ils ont été découverts au cours du 20ème siècle, tout d’abord chez des animaux (volailles, porcs, souris) et puis chez les humains dans les années 60. Actuellement on connait plus de 5000 variétés de coronavirus, mais seulement sept sont susceptibles de s’attaquer aux humains. Quatre d’entre eux entraînent de simple rhumes sans gravité, mais les trois suivants peuvent provoquer des maladies respiratoires graves et c’est donc le cas du SARS-CoV-2 qui est apparu en Chine à la fin de l’année dernière et est à l’origine de la maladie Covid-19.
Gauche : Une représentation du SARS-CoV-2 par David Goodsell
Droite : Une image (Wikipedia) de coronavirus prise au microscope électronique.
SARS-CoV-2 est un virus à ARN, son matériel génétique consiste donc en un unique long brin d’ARN comprenant environ 30 000 bases nucléiques (ce qui est 10 000 fois plus court que le génome humain). Le génome du SARS-CoV-2 a été séquencé dès le mois de janvier 2020, et on sait qu’il code pour 29 protéines. Parmi celles dont la fonction a été identifiée, certaines servent à reproduire le matériel génétique du virus, d’autres à former l’enveloppe qui va protéger celui-ci, ou encore à camoufler l’activité virale au sein de la cellule afin que celle-ci ne puisse pas déclencher son système de défense (dans les films de braquage ce serait le geek qui va hacker les caméras de surveillance pour que ses petits camarades puissent bosser en toute discretion). Bref, on a affaire à une équipe de professionnels !

Depuis le début de la crise sanitaire, les équipes de recherche en biochimie structurale sont à pied d’oeuvre, et plus d’une centaine de structures protéiques sont déjà disponibles sur la PDB (attention ça ne concerne pas toutes les protéines du virus, puisque pour certaines d’entre elles plusieurs structures différentes sont disponibles). Actuellement deux protéines sont plus particulièrement sous le feu des projecteurs :
- La protéine S (comme spike, soit pointe en anglais), c’est celle qui forme des protubérances à surface de l’enveloppe virale (en rose clair dans l’illustration de Goodsell postée plus haut). On sait désormais qu’il s’agit un peu du bras armé du virus, et c’est son interaction avec le récepteur ACE2 (une protéine que l’on trouve à la surface de la membrane cellulaire humaine), qui va permettre au virus de pénétrer la cellule cible. Et comme ACE2 est plus particulièrement exprimée dans les cellules pulmonaires, on comprend mieux pourquoi ce virus provoque des problèmes respiratoires. La protéine S représente une cible potentielle dans les travaux visant à développer un vaccin contre le virus. L’objectif serait donc d’aider notre organisme à fabriquer des anticorps capable de l’identifier et de la neutraliser avant que les cellules soient infectées.

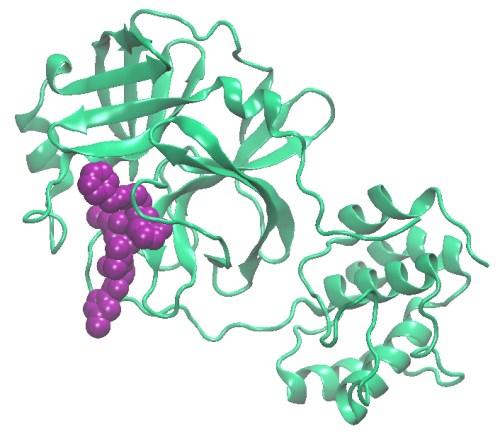
- La protéase principale (car le virus en produit plusieurs) a pour mission de couper la chaîne peptidique continue produite lors de l’étape de traduction ARN → protéine en plusieurs morceaux peptidiques fonctionnels. C’est une des cibles potentielles des antiviraux qui sont en cours de développement contre la maladie.
Pour en savoir plus :
- Bad news wrapped in proteins (en anglais), un très bon article du New-York Times (du 03/04/2020) qui passe en revue les protéines codées par le génome du SARS-CoV-2.
- Un article de Nicolas Doucet, un chercheur québecois (en français donc), sur l’interaction entre une protéine du SARS-CoV-2 et les protéines humaines.
- L’ensemble des ressources (et notamment les structures protéiques) disponibles sur le SARS-CoV-2 sur la PDB (en anglais, mis à jour au fur et à mesure).


