Dans les tout débuts de ce blog, nous vous avons parlé des virus, et de leur fâcheuse tendance à détourner la machinerie protéique de la cellule qu’ils infectent pour reproduire leur propre matériel génétique. Ledit matériel génétique peut être constitué d’ADN (comme pour la varicelle), qui devra donc être transcrit en ARN, qui sera lui-même traduit en protéine par le ribosome, ou bien d’ARN (comme pour la grippe ou le terrible coronavirus) et dans ce cas on peut passer directement à la case ribosome pour produire des protéines virales.
Et puis dans la famille des virus à ARN, on trouve aussi une bande de petits rebelles qui ont décidé de ne rien faire comme les autres, ce sont les rétrovirus. Chez les rétrovirus, on ne se contente pas bêtement de squatter le ribosome du voisin, non, non, non. Dans cette famille là on a décidé de voir plus grand et d’infecter durablement les cellules en modifiant leur patrimoine génétique. Et pour ce faire, les rétrovirus disposent de deux enzymes de destruction massive, la transcriptase inverse et l’intégrase.
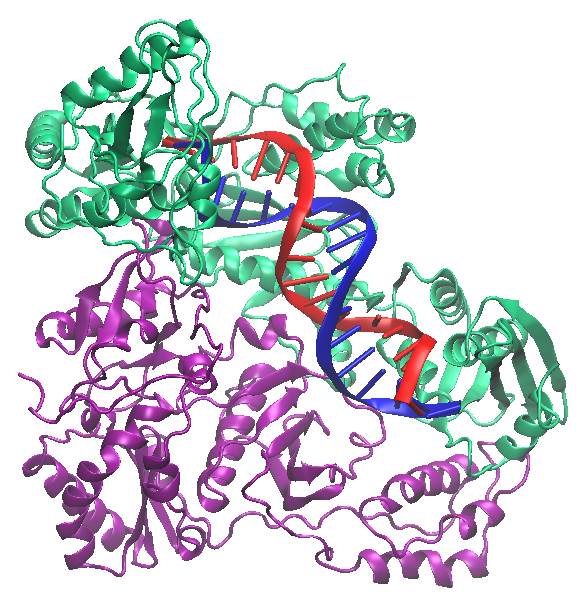
- La transcriptase inverse est capable de synthétiser de l’ADN à partir de l’ARN viral. Sauf que contrairement à l’ADN polymérase qui aime travailler proprement et ne fait que très rarement des erreurs, lorsqu’elle se charge de dupliquer notre ADN, la transcriptase inverse, elle, travaille comme un cochon et se trompe environ toutes les 2000 bases (soit 5 millions de fois plus souvent). Mais cette approche brouillonne n’est pas le fruit du hasard et nous allons voir qu’elle sert en fait les intérêts du rétrovirus. En effet ce fort taux d’erreur permet de produire rapidement de nouveaux variants du virus, qui en quelque semaines sera à même de résister au traitement initial. Pour lutter efficacement contre un rétrovirus il faut donc le prendre de vitesse, via un traitement incluant plusieurs molécules, afin qu’il ne puisse pas simultanément développer de résistance à toutes. Cette variabilité génétique des rétrovirus rend également difficile la conception de vaccins, puisque les antigènes à cibler sont susceptibles de changer au fur et à mesure de l’évolution du génome du rétrovirus. La transcriptase inverse est une enzyme multifonctionnelle, puisqu’elle possède donc un site de type polymérase, qui a pour mission de synthétiser de l’ADN à partir d’un modèle en ARN, mais également un site de type nucléase, qui va lui se charger de réduire en pièce détachée l’ARN viral après utilisation. il s’agit donc d’un malfaiteur qui prend soin d’effacer ses traces après son forfait…

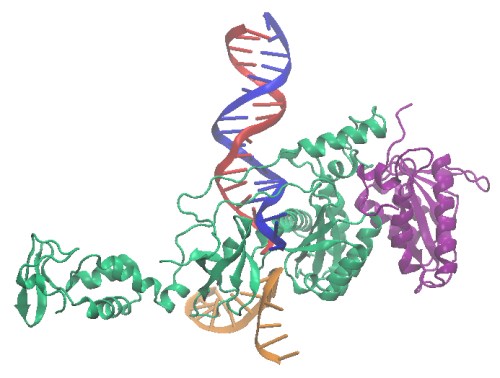
- Dans un second temps, l’intégrase va se charger d’intégrer l’ADN ainsi fabriqué au génome de la cellule infectée. Le matériel génétique du rétrovirus est alors présent de manière permanente dans cette cellule, et si elle vient à se diviser, il sera alors transmis à l’ensemble des cellules filles. Qui plus est, une cellule infectée peut parfaitement continuer à vivre paisiblement sa vie sans initialement produire de protéines virales, mais en se multipliant. On aura alors toute une population cellulaire porteuse de matériel génétique viral dormant, qui pourra peut-être un jour s’exprimer, ou peut-être jamais. Cette caractéristique des infections par rétrovirus les rend également particulièrement coriaces à combattre. Par ailleurs, on estime près de 8% du génome humain serait d’origine rétrovirale, certains fragments d’ADN viral nous ayant été transmis par nos ancêtres pendant plusieurs millions d’années d’évolution. La syncitine, qui est une protéine jouant un rôle clé dans la formation du placenta durant la grossesse, est ainsi d’origine virale. Comme quoi une cohabitation paisible avec les petits squatteurs est parfois possible !
Le plus (tristement) célèbre des rétrovirus est sans doute le VIH, contre lequel les chercheur·se·s s’efforcent de développer des antirétroviraux, qui cibleront justement ces deux enzymes, via des inhibiteurs qui vont entraver leur bon fonctionnement.
Mais les rétrovirus sont aussi une source d’espoir pour la recherche médicale, car leur capacité à intégrer de l’ADN dans le génome d’une cellule cible pourrait être exploitée dans cadre de thérapies géniques et la comprehension approfondie de leur fonctionnement représente donc une perspective intéressante pour la luttes contre les maladies génétiques.
Pour en savoir plus :
La transcriptase inverse et l’intégrase ont toutes deux été molécules du mois sur la PDB en septembre 2002, et en mars 2011.