Que ce soit dans une canette de soda ou une flute de champagne, les petites bulles qui égayent nos boissons gazeuses sont dues à la présence d’acide carbonique dissous dans le liquide, et qui va s’échapper sous forme de dioxyde de carbone gazeux selon la réaction suivante :
H2CO3 = CO2 + H20
Cette réaction est cependant assez lente, ce qui va permettre à votre boisson préférée de conserver ses bulles pendant quelques jours (surtout si vous gardez celle-ci au frais). Pourtant, dès que vous prenez une gorgée en bouche, les bulles disparaissent en quelques secondes. C’est parce que l’acide carbonique est entré en contact avec un enzyme contenue dans notre salive, l’anhydrase carbonique, et celle-ci catalyse justement la réaction d’interconversion entre l’acide carbonique et le dioxyde de carbone (dans un sens ou dans l’autre, selon les circonstances).
Bien entendu cette enzyme n’a pas pour fonction principale d’éventer votre champagne, on la rencontre en divers endroits du corps humain (et dans de nombreux autres organismes), où elle sera tout à fait cruciale. En vrai, son job est de réguler le pH des cellules en catalysant la réaction soit dans le sens de production de l’acide carbonique, soit vers la production de dioxyde de carbone. Cette protéine est notamment présente dans la muqueuse de l’estomac, où elle servira à produire de l’acide nécessaire à notre digestion des aliments. Elle joue également un rôle dans la régulation de la quantité d’eau dans les yeux, et certains glaucomes (une pathologie associée à une trop grande pression oculaire due à un excès d’eau) peuvent ainsi être traités via un inhibiteur de l’anhydrase carbonique.
Dans les plantes cette enzyme permet aussi le stockage du dioxyde de carbone sous forme d’ions bicarbonates, en attendant son exploitation par Rubisco lors de la photosynthèse. Mais contrairement à Rubisco, qui est connue comme l’escargot du monde protéique, l’anhydrase carbonique est plutôt du genre guépard, et se caractérise par une vitesse de réaction remarquable puisqu’elle peut convertir jusqu’à un million de molécules par seconde.
Enfin l’anhydrase carbonique est essentielle dans le cycle respiratoire. En contrôlant le pH des cellules elle permet de moduler l’affinité de l’hémoglobine pour le dioxygène, qui sera ainsi fixé au niveau des poumons et ensuite relâché dans les organes qui en ont besoin. Cette enzyme contrôle également l’évacuation du dioxyde de carbone produit par nos cellules. En effet, seulement 20% de celui-ci a la chance de monter à bord du petit train de l’hémoglobine pour être acheminé en mode VIP vers nos poumons. Dans 70% des cas les molécules de CO2 seront simplement converties en acide carbonique et voyageront en classe éco dans le flux sanguin. Une fois arrivées à destination, l’anhydrase carbonique se charge de les retransformer en dioxyde carbone qui sera expulsé lors de la respiration.
Cette protéine a été découverte dès 1933, mais l’on a bien vite constaté qu’il s’agissait plutôt d’une famille d’enzymes, que l’on rencontre dans des organismes variés (mammifères, plantes, algues ou bactéries), et qui sont distribuées en trois grands groupes (alpha, beta et gamma).
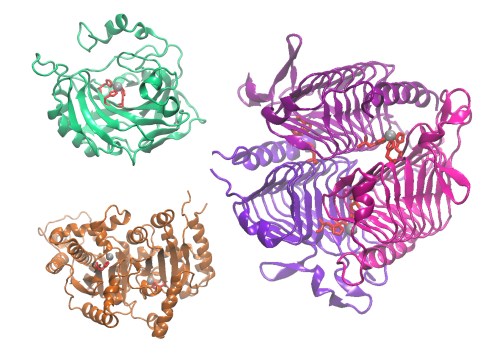
Trois exemples d’anhydrases carboniques issues de l’homme (en vert, pdb 1ca2), d’une algue (en orange, pdb 1ddz) et d’une bactérie thermophile (en violet, pdb 1thj). Elles présentent des formes et des tailles variées, mais toutes comportent des atomes de zinc (en gris) maintenus en place par des acides aminés de type histidine (en rouge)
Les anhydrases carboniques présentent des structures très diverses (ce qui en fait donc un très bon exemple d’évolution convergente), mais elles ont toutes pour point commun de posséder en leur coeur un ou plusieurs atomes de zinc qui sont indispensables au bon déroulement de la réaction chimique. Au sein d’un même organisme on peut également observer différents variants, dont l’activité est adapté à l’organe où ils sont exprimés. Les anhydrases carboniques présentes dans nos fibres musculaires sont ainsi beaucoup moins rapides que celles présentes dans notre salive. Quoiqu’il en soit, la prochaine fois que des bulles viendront vous picoter la langue, prenez le temps de penser à cette enzyme !
Pour en savoir plus :
- L’anhydrase carbonique a été la molécule du mois sur la PDB (en anglais)

Bonjour pouvez vous me donner une adresse pour me procurer de l handryaze carbonique pour réduire mes apnée du sommeil
Cordialement
J’aimeJ’aime