Le vivant possède la faculté fascinante de se développer dans des conditions extrêmes qui pourraient sembler insoutenables aux pauvres organismes tempérés que nous sommes.
C’est ainsi que les sources hydrothermales découvertes au fonds des océans il y a près d’une demi-siècle, et où l’eau peut atteindre plus de 300°C en jaillissant, abritent tout un écosystème d’organismes thermophiles, voire hyperthermophiles, qui se sont spécifiquement adaptés à la vie à haute température. On soupçonne d’ailleurs les premiers organismes vivants, d’avoir vu le jour (enfin plutôt la nuit, puisqu’il y règne une obscurité complète) dans cet environnement très particulier.
À l’autre bout du spectre thermal, on trouve les organismes psychrophiles, qui ont élu domicile dans les environnements (très) froids : Mers polaires, où la température est inférieure à 5°C, abysses (sans sources pour réchauffer l’ambiance cette fois) ou glaciers. Ces organismes passionnent également les chercheur·se·s, car ils ont développé une catégorie de protéines bien à eux, les protéines antigels, dites aussi AFPs (pour Anti Freeze Proteins). Comme leur nom l’indique assez clairement, les AFPs ont pour mission d’empêcher la croissance à l’intérieur des cellules de cristaux de glace qui pourraient détériorer celles-ci en déchirant la membrane cellulaire. Lorsqu’un un petit cristal de glace apparaît, les AFP vont former un cordon de sécurité autour de celui-ci, telles une armée de petits gardes du corps, empêchant ainsi d’autres molécules d’eau de le rejoindre et le cristal de grossir.
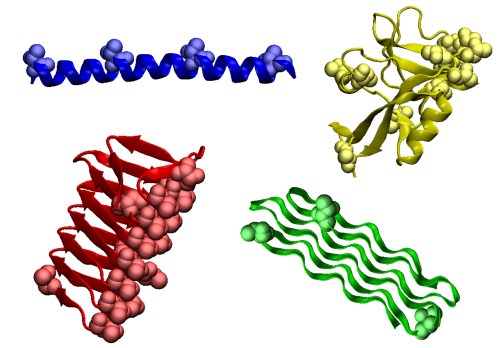
On trouve des protéines antigels dans de nombreuses espèces, poissons, plantes ou insectes, et celles-ci peuvent aussi présenter une grande variété de structures, en hélices α ou en solénoïdes β (où les feuillets β s’enroulent eux-même en hélice, comme dans l’exemple en rouge de la figure plus haut). Elles représentent donc un exemple frappant d’évolution convergente, où des espèces distinctes, mais soumises à des contraintes environnementales similaires (résister au froid et au risque de détérioration de cellules associé) ont développé indépendamment des réponses semblables.

Les AFPs ouvrent aussi de nombreuses perspectives en biotechnologies, que ce soit pour améliorer la résistance au froid d’un organisme, le stockage à basse température de tissus vivants (par exemple en attente d’une greffe), mais aussi l’amélioration de la durée de vie des produits surgelés. C’est d’ailleurs dans l’agro-alimentaire que les protéines antigels ont récemment connu leur heure de gloire. Le géant Unilever a en effet décidé d’introduire des protéines antigels de la loquette (un poisson vivant dans les eaux froides de l’Atlantique Nord) dans une de ses crèmes glacées, afin d’y éviter la formation de cristaux de glace (les petites paillettes qui nuisent à l’onctuosité de la crème quand celle-ci a été un peu trop décongelée puis recongelée).
Mais que les gastronomes se rassurent, le poisson ne figure dans la liste des ingrédients nécessaires pour préparer la crème glacée, puisque la protéine utilisée est intégralement produite par une levure génétiquement modifiée.
