En théorie, le repliement de la chaîne protéique à la sortie du ribosome peut se faire de manière autonome et spontanée, comme si notre molécule était un petit origami autopliant. Néanmoins, dans certains cas, comme des protéines particulièrement volumineuses, ou des assemblages complexes comprenant plusieurs chaînes, la protéine nouvellement produite va être assistée dans son repliement par un chaperon. En effet, la plupart des protéines contiennent dans leur séquence des domaines composés de résidus hydrophobes. Une fois la chaîne correctement repliée, ces résidus vont se retrouver au centre de la structure tertiaire, loin du solvant aqueux, formant ainsi ce que l’on appelle le coeur hydrophobe de la protéine. Mais avant que le repliement ne soit achevé, les domaines hydrophobes d’une protéine sont susceptibles d’interagir entre eux et de former des agrégats, c’est à dire des amas de protéines à la structure incorrecte et qui peuvent s’avérer être toxiques pour notre organisme.

Les protéines chaperons, connues depuis maintenant une quarantaine d’années, permettent de faciliter le repliement correct, c’est-à-dire dans leur forme fonctionnelle, des protéines, notamment en les isolant des partenaires potentiellement indésirables qui peuvent être nombreux, car le milieu cellulaire est extrêmement encombré (on peut s’en faire une petite idée en regardant les représentation de l’intérieur d’une cellule par David Goodsell). Les protéines chaperons peuvent également veiller au bon assemblage des protéines au sein d’un complexe macromoléculaire, mais sans prendre part à la structure finale du complexe. Donc pour résumer la situation, la mission des protéines chaperons est de prévenir les interactions incorrectes entre protéines, que ce soit en tant que duègnes ou comme marieuses, avouez que leur nom a été plutôt bien trouvé non ?

En temps normal, seules 10 à 20% des protéines nécessitent l’assistance d’un chaperon pour leur repliement. Mais les chaperons peuvent également être appelés à la rescousse (et par conséquent produits en grande quantité par la cellule) en cas de perturbation environnementale : changement de température, exposition à une toxine ou au stress oxydant. Ces modifications du milieu cellulaire sont susceptibles de dénaturer les protéines, ce qui leur fait ainsi perdre leur activité biologique et facilite leur agrégation.
Un grand nombre de chaperons (mais pas tous) appartiennent ainsi à la famille des HSP (Heat Shock Proteins), les protéines de choc thermique, découvertes, comme leur nom le laisse supposer, après une expérience où des cellules étaient soumises à de fortes variations de température. Cette brigade d’élite débarque pour remettre de l’ordre et protéger la cellule en cas de grosse chaleur, mais aussi de coup de froid, ou encore d’exposition à des radiations UV. La plupart des chaperons permettent un repliement correct des chaînes dépliées dans des conditions dégradées, mais certaines peuvent également réparer les dégâts dus au stress. HSP100 est ainsi capable de déplier une protéine qui aurait adopté une structure incorrecte, avant de la replier dans sa forme native. HSP104 pour sa part, peut resolubiliser les protéines impliquées dans des agrégats, les ramenant ainsi dans le droit chemin de leur état natif.
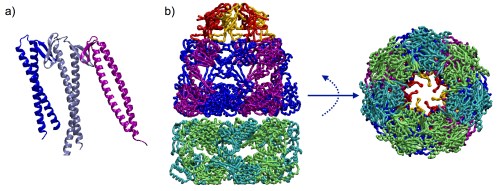
Il existe une grande variété, en forme et en taille, de protéines chaperons. Côté petits formats, on peut mentionner la préfoldine avec sa jolie forme de pieuvre, qui va protéger les chaînes protéiques des contacts indésirables juste à leur sortie du ribosome. À l’autre bout de l’échelle, on trouve l’énorme complexe GroEl/GroES, qui est composé de 21 sous-unités, et forme une cavité suffisamment spacieuse pour qu’une protéine puisse s’y replier confortablement. GroEl/GroEs va ainsi avaler les chaînes protéiques dépliées, et puis les recracher une fois que celles-ci ont adopté leur conformation native en son sein. Si certains chaperons veillent spécifiquement aux bonnes fréquentations d’une protéine donnée, d’autres sont moins regardants quant aux protéines qu’ils vont assister. GroEl/GroEs par exemple contribue au bon repliement de plus de 80 protéines différentes.

Mais qui va replier les chaperons ?
Si les chaperons sont les grues qui assistent le montage des structures et assemblages protéiques, la question que l’on se pose spontanément est celle de leur propre repliement. Les chaperons de petite taille sont capables de se replier tous seuls comme des grands (!). Quant aux gros systèmes, ils peuvent effectivement s’auto-chaperonner. Le complexe GroEL-GroEs peut ainsi procéder au repliement des chaînes constitutives de ses sous-unités, chaînes qui, une fois relâchées dans le cytoplasme, vont s’assembler, toujours avec l’aide de GroEl-GroEs, pour former un nouvel exemplaire de ce complexe.
